En 2025, l’ESC et l’EAS ont proposé une actualisation des recommandations de 2019 pour la prise en charge des dyslipidémies, nécessaire du fait de plusieurs données nouvelles. Elle peut se résumer à trois grands principes.
Premier principe : évaluer le risque
L’évaluation du risque cardiovasculaire (CV), qualifié normativement en degré de sévérité, a trois composantes.
Première composante : utiliser des moyens simples
Si le message paraissant clef et le plus souvent retenu est d’utiliser les grilles de risque SCORE2, il doit être relativisé car le recours à ces grilles est de fait limité. Ainsi, le risque n’est pas quantifié mais qualifié en degré de sévérité (très élevé, élevé, intermédiaire et faible) et le recours aux grilles SCORE2 quantifie un risque qui doit ensuite être qualifié. Ainsi, avant de recourir aux grilles SCORE2, des marqueurs simples doivent être utilisés pour qualifier le risque (voir tableaux 1 à 3)
Ensuite, seules les grilles SCORE2 et SCORE2- OP (pour les personnes de plus de 70 ans) doivent être utilisées et non pas la grille SCORE2-diabetes, le diabète étant inclus dans les catégories de risque.
Enfin, les grilles SCORE2 ne doivent être utilisées que chez des patients en prévention primaire ne recevant pas de traitement hypolipémiant et elles ne doivent plus l’être pour de nouvelles évaluations chez un même patient.
Deuxième composante : affiner si nécessaire
Dans certains cas, il est possible d’utiliser des marqueurs permettant de mieux qualifier le risque, que ce soit l’existence de comorbidités (maladies inflammatoires, obésité…), d’une imagerie non invasive (échodoppler, score calcique) ou de biomarqueurs (hsCRP, Lp(a)) (voir tableau 4).
Si cette approche est logique, elle reste encore mal définie quant aux sujets à laquelle elle doit s’appliquer (en principe, les sujets à risque intermédiaire), quant aux marqueurs à utiliser préférentiellement (et aucun ne semble privilégié) ou en association (faut-il faire un score calcique chez un sujet ayant une maladie inflammatoire stabilisée et peu active ?), quant au seuil en faisant un critère de reclassification du risque (comme par exemple, les valeurs du score calcique à prendre en compte) et quant aux niveaux de correction du risque à apporter (ainsi, si la hs-CRP est supérieure à 2, le risque doit être considéré comme augmenté, mais cela veut-il dire que le sujet augmente d’une catégorie ou que son risque s’accroit d’un certain
pourcentage, sans pour autant le faire changer de catégorie de risque ?)
Troisième composante : le niveau de risque fixe la cible lipidique
Ici, les propositions rejoignent celles des recommandations précédentes : le LDL-c doit être d’autant plus diminué que le risque est élevé avec une cible inférieure à 0,55 g/l en cas de très haut risque, inférieur à 0,70 g/l en cas de haut risque, inférieure à 1,00 en cas de risque intermédiaire, inférieure à 1,16 g/l en cas de risque faible.
Il apparait une catégorie d’extrême risque pour laquelle la cible de LDL-c doit être inférieure à 0,40 g/l et qui a une définition simple avec deux catégories : patients en prévention secondaire faisant une récidive d’événement CV alors qu’ils sont à la dose maximale tolérée de statines, et patients ayant une maladie polyvasculaire.
Deuxième principe : utiliser tous les traitements diminuant le LDL-c
L’abaissement du LDL-c au prorata du niveau de risque reste l’objectif prioritaire et les statines restent le traitement de référence. Mais il est reconnu que tous les traitements au bénéfice clinique validé peuvent être associés et ce, même en l’absence de traitement par statine, chacun apportant un bénéfice clinique au prorata de la diminution du LDL-c qu’il permet.
Ainsi, peuvent être utilisés, les statines, l’ézétimibe, l’acide bempédoïque et les anticorps monoclonaux anti-PCSK9 (et donc pas l’inclisiran, non disponible en France par ailleurs).
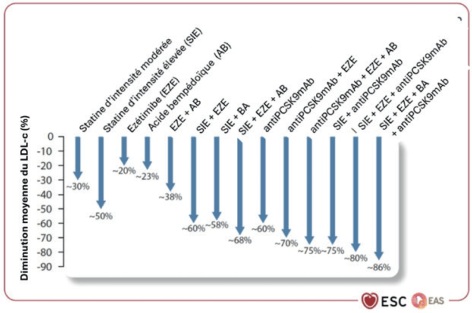
La diminution relative du LDL-c permise par ces traitements seuls ou en association a été illustrée par un schéma (figure 1)
Troisième principe : des stratégies définies selon certaines situations cliniques
La stratégie de prise en charge des paramètres lipidiques est précisée dans certaines situations cliniques.
Dans le syndrome coronaire aigu
Le principe est de faire en sorte que le patient quitte le milieu hospitalier avec un traitement qui devrait lui permettre d’atteindre la cible lipidique et la stratégie proposée est la suivante :
- Intensifier le traitement dès l’hospitalisation initiale pour les patients qui recevaient n’importe quel traitement hypolipémiant avant l’hospitalisation pour diminuer plus encore leur LDL-c ;
- Débuter une association comprenant une statine fortement puissante et de l’ézétimibe durant l’hospitalisation initiale pour SCA chez les patients ne recevant pas antérieurement d’hypolipémiant et dont il est envisageable que la cible lipidique ne sera pas atteinte sous une monothérapie
Dans l’infection par le VIH
Une étude, REPRIEVE, a démontré que la pitavastatine réduit significativement et précocement le risque CV de patients infectés par le VIH. De ce fait, un traitement par statine est recommandé en prévention primaire chez les patients âgés d’au moins 40 ans, infectés par le VIH, indépendamment de leur niveau de risque CV et de leur taux de LDL-c, pour réduire le risque d’événements CV ; le choix de la statine doit reposer sur l’étude des interactions potentielles avec les autres traitements de ces patients.
Les auteurs ajoutent que, bien que des essais thérapeutiques d’autres hypolipémiants n’ont pas été conduits chez des patients infectés par le VIH, des données sur la réduction du LDL-c et la tolérance de l’ézétimibe et des antiPCSK9 (mAb) sont disponibles, permettant leur utilisation.
Cancer
L’étude STOP-CA a été la seule parmi quatre, à démontrer qu’une statine (l’atorvastatine à 40 mg/j) peut diminuer la cardiotoxicité d’un traitement par anthracyclines, chez des patients ayant un lymphome. De ce fait, et pour être en accord avec les recommandations européennes de cardio-oncologie de 2022, les auteurs ont proposé que les statines puissent être envisagées chez les adultes à haut ou très haut risque de développer une toxicité cardiaque de la chimiothérapie pour réduire le risque de dysfonction cardiaque induit par les anthracyclines.
Surveillance
Enfin, un principe simple : lorsqu’une stratégie hypolipémiante a été débutée ou modifiée, un bilan lipidique doit être effectué dans les 4 à 6 semaines qui suivent pour en vérifier l’efficacité et ajuster le traitement.
Tableau 1
Catégories de risque ESC-EAS 2025
Classification – données qualitatives
Très haut risque : n’importe lequel des éléments suivants
- maladie CV documentée, clinique ou sans équivoque en imagerie :
- antécédent de SCA (IDM ou angor instable), syndrome coronaire chronique, revascularisation coronaire ou artérielle, AVC ou AIT et maladie artérielle périphérique;
- maladie CV sans équivoque en imagerie = éléments prédictifs d’événements cliniques comme des plaques significatives en coronarographie ou coroscanner ou en échodoppler carotide ou des artères fémorales ou une élévation marquée du score calcique coronaire.
- diabète sucré
- avec atteinte d’un organe cible ou au moins 3 autres facteurs de risque CV majeurs
- ou diabète de type 1 ayant début précocement ou dont la durée est d’au moins 20 ans
- maladie rénale chronique sévère (DFGe < 30ml/min/1,73m2)
- risque calculé avec le SCORE2 ou le SCORE2-OP à au moins 20%
- hypercholestérolémie familiale avec une maladie CV ou un autre facteur de risque majeur
Tableau 2
Catégories de risque ESC-EAS 2025
Classification – données qualitatives
Haut risque : n’importe lequel des éléments suivants
- un seul facteur de risque CV nettement élevé, notamment un cholestérol total (CT) supérieur à 3,10 g/l ou un LDL-c supérieur à 1,90 g/l ou une pression artérielle supérieure à 180/110 mm Hg
- hypercholestérolémie familiale sans autre facteur de risque majeur
- diabète sucré sans atteinte d’un organe cible dont la durée est d’au moins 10 ans ou ayant un autre facteur de risque CV additionnel
- maladie rénale chronique modérée (DFGe entre 30 et 59 ml/min/1,73 m2)
- risque calculé avec le SCORE2 ou le SCORE2-OP compris entre au moins 10% et moins de 20%
Tableau 3
Catégories de risque ESC-EAS 2025
Classification – données qualitatives
Risque intermédiaire ou modéré : n’importe lequel des éléments suivants
- patient jeune (diabète de type 1 avant 35 ans ; diabète de type 2 avant 50 ans) et dont la durée du diabète est inférieure à 10 ans, sans autre facteur de risque CV majeur
- risque calculé avec le SCORE2 ou le SCORE2-OP compris entre au moins 2% et moins de 10%
- diabète sucré sans atteinte d’un organe cible dont la durée est d’au moins 10 ans ou ayant un autre facteur de risque CV additionnel
Risque faible : SCORE2 ou SCORE2-OP inférieur à 2%
Tableau 4
Facteurs de modulation
Données démographiques ou cliniques
- Antécédents familiaux de maladie CV précoce (hommes < 55 ans, femmes < 60 ans)
- Origine ethnique à haut risque (par exemple, Asie du sud)
- Symptômes de stress ou stress psychosocial
- Faible niveau socio-économique
- Obésité
- Inactivité physique
- Maladie chronique auto-immune ou inflammatoire
- Troubles psychiatriques majeurs
- Ménopause précose
- Pré-éclampsie ou autre désordre hypertensif pendant la grossesse
- Infection par le VIH
- Syndrome d’apnées obstructives du sommeil
Biomarqueurs
- Élévation persistante de la hs-CRP (>2mg/l)
- Lp(a) élevé (>50mg/dl ou >105 nmol/l)
Laissé à l’appréciation du médecin
Essentiellement quand patient en zone intermédiaire ou à risque intermédiaire pour aider à la prise de décision
Figure 1
Diminution relative moyenne du LDL-c
selon les traitements et leurs associations